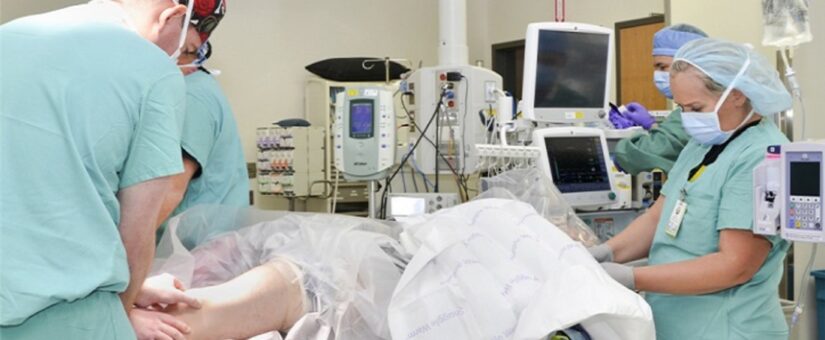
COVID-19 Gyorsreagálású FDA megfelelés orvostechnikai eszköz gyártók részére
- On 2020.03.31.
A COVID-19 elleni intézkedésekre összpontosító gyártóknak a következőket kell tudniuk.
Az Élelmiszer- és Gyógyszerügyi Hivatal (FDA) intézkedéseket hozott, hogy a COVID-19 elleni intézkedéseket fejlesztő orvostechnikai eszköz gyártók számára gyorsított lehetőséget biztosítson az FDA engedélyezés és a felelősség alóli mentesség megszerzésére.
(Ez a cikk kizárólag oktatási célokat szolgál, és nem jogi vagy üzleti tanácsadás nyújtására készült.)
Alapvető tudnivalók
Először is fontos ismerni orvostechnikai eszköz termékének FDA besorolását. Három orvostechnikai eszköz osztály létezik: I., II. és III. osztály. Röviden, ezek az osztályok a páciensre jelentett kockázat szintjével emelkednek, és ennek megfelelően nő a szükséges megfelelőségi szint. Az I. osztályba jellemzően olyan eszközök tartoznak, mint a nyelvlapocok és az ortopédiai rögzítők, míg a III. osztályba olyanok, mint a szívimplantátumok és az automata defibrillátorok. Érdekesség, hogy az N95 maszkok a II. osztályba tartoznak.
Az orvostechnikai eszköz gyártóknak regisztrálniuk kell létesítményüket és listázniuk kell termékeiket az FDA-nál. Általánosságban elmondható, hogy egy orvostechnikai eszköz valószínűleg ugyanabba az osztályba fog tartozni, mint a piacon lévő hasonló vagy összehasonlítható, már létező termékek. Bevett gyakorlat a felhasznált besorolási indoklás dokumentálása. Az innovatív új termékeknek, amelyekhez nincs összehasonlítható termék, egy de novo igénylési folyamaton kell keresztülmenniük, amellyel itt nem foglalkozunk.
Vészhelyzeti intézkedések
Az FDA 2020. március 24-én bevezette a sürgősségi felhasználási engedélyek (EUA) alkalmazását a COVID-19 kezelésére szolgáló orvostechnikai eszközök három kategóriájának regisztrációjának és sürgősségi jóváhagyásának megkönnyítése érdekében. Az EUA-k a COVID-19-re irányuló alternatív vagy módosított orvostechnikai eszközök sürgősségi felhasználására is vonatkoznak.
Az EUA-k által lefedett orvostechnikai eszközök három kategóriája a következő:
- Lélegeztetőgépek
- Személyi védőfelszerelések (PPE)
- In vitro diagnosztika
Ezen terméktípusokhoz EUA kérelmet kell benyújtani. Jóváhagyás esetén az FDA egy engedélyező levéllel válaszol.
Az I. osztályú orvostechnikai eszközök esetében az EUA folyamat a normál I. osztályú regisztrációs folyamat enyhe egyszerűsítését jelenti, amely nem vészhelyzeti körülmények között jellemzően gyors volt. A II. osztályú eszközök esetében az EUA-k valószínűleg gyorsabb utat kínálnak az FDA piaci engedélyének megszerzéséhez.
Felelősség elleni védelem
Az EUA-kon kívül az Egészségügyi és Humán Szolgáltatások Minisztériuma (HSS) 2020. február 4-én hatályba lépő nyilatkozatot adott ki a Közegészségügyi Készenléti és Vészhelyzeti Felkészültségi (PREP) törvény értelmében a COVID-19 elleni orvosi ellenintézkedésekkel kapcsolatos tevékenységekre vonatkozó felelősség alóli mentesség biztosítása érdekében. A PREP törvényt eredetileg 2005-ben fogadták el, hogy felelősségvédelmet biztosítson a vakcinák gyógyszergyártóinak közegészségügyi válság idején. Azonban a 2020. február 4-i nyilatkozattal a felelősség alóli mentesség kiterjedt a COVID-19 elleni fedezett ellenintézkedéseket fejlesztő orvostechnikai eszköz gyártókra is.
Altemir Consulting
Az Altemir Consulting számos gyártóipari vállalkozásra fókuszál, beleértve az orvostechnikai eszközök szabályozási megfelelőségére való szakosodást is. Lépjen kapcsolatba velünk, hogy többet megtudjon.